Mis on hõbepeegli reaktsioon? Keemiline katse: hõbepeegli saamine Hõbepeegli reaktsiooni tingimused
Eksperiment klaasile peeglikatte moodustamise kauni efektiga on väga visuaalne. See reaktsioon nõuab kogemust ja kannatlikkust. Sellest artiklist saate teada seadmete vajaliku ja spetsiifilise ettevalmistamise kohta ning näete ka seda, milliste reaktsioonivõrranditega see protsess toimub.
Hõbepeegli reaktsiooni olemus on metallilise hõbeda moodustumine redoksreaktsiooni tulemusena hõbeoksiidi ammoniaagilahuse interaktsiooni käigus aldehüüdide juuresolekul.
"Silver Mirror" (katseklaas vasakul)Vastupidava hõbedakihi loomiseks vajate:
- klaaskolb mahuga kuni 100 ml;
- ammoniaagilahus (2,5-4%);
- hõbenitraat (2%);
- formaldehüüdi vesilahus (40%).
Selle asemel võite võtta valmis Tollensi reaktiivi - ammoniaagi lahus hõbeoksiid. Selle loomiseks peate 10 tilga veele lisama 1 grammi hõbenitraati (kui vedelikku hoitakse pikka aega, peate selle asetama pimedasse kohta või tumedate seintega klaasnõusse). Vahetult enne katset tuleb lahus (umbes 3 ml) segada vahekorras 1:1 naatriumhüdroksiidi 10% vesilahusega. Hõbe võib sadestuda, seetõttu lahjendatakse seda aeglaselt ammoniaagilahuse lisamisega. Soovitame teha veel ühe suurejoonelise katse ammoniaagilahusega ja printida “keemiline foto”.
Reaktsioon viiakse läbi kl toatemperatuuril. Nõutav tingimus edukas finaal on klaasanuma täiesti puhtad ja siledad seinad. Kui seintel on vähimadki saasteainete osakesed, muutub katse tulemusena saadud sete lahtiseks musta või tumehalli värvi kihiks.
Kolvi puhastamiseks peate kasutama erinevad tüübid leeliselahused Seega võib töötlemiseks võtta lahuse, mis pärast puhastamist tuleb destilleeritud veega maha pesta. Puhastusvahendi kolbi on vaja mitu korda loputada.
Miks on laeva puhtus nii oluline?
Fakt on see, et katse lõpus moodustunud kolloidhõbedaosakesed peavad klaasi pinnale kindlalt kinni jääma. Selle pinnal ei tohiks olla rasva ega mehaanilisi osakesi. vesi ei sisalda sooli ja sobib ideaalselt kolvi lõplikuks puhastamiseks. Seda saab valmistada kodus, kuid lihtsam on osta valmis vedelikku.
Hõbepeegli reaktsioonivõrrand:
Ag₂O + 4 NH₃·Н₂О ⇄ 2ОН + 3Н₂О,
kus OH on diamiinhõbehüdroksiid, mis saadakse metalloksiidi lahustamisel ammoniaagi vesilahuses.
 Diamiin hõbeda kompleksmolekul
Diamiin hõbeda kompleksmolekul
Tähtis! Reaktsioon toimib madalal ammoniaagi kontsentratsioonil - jälgige hoolikalt proportsioone!
Reaktsiooni viimane etapp kulgeb järgmiselt:
R (mis tahes aldehüüd)-CH=O + 2OH → 2Ag (sadestunud hõbekolloid) ↓ + R-COONH₂ + 3NH₃ + H2O
Parem on läbi viia reaktsiooni teine etapp, kuumutades kolbi ettevaatlikult põleti leegi kohal - see suurendab katse õnnestumise tõenäosust.
Mida võib näidata hõbedase peegli reaktsioon?
See huvitav keemiline reaktsioon ei näita mitte ainult aine teatud olekuid – seda saab kasutada aldehüüdide kvalitatiivseks määramiseks. See tähendab, et selline reaktsioon lahendab küsimuse: kas lahuses on aldehüüdrühm või mitte.
 Aldehüüdide üldine struktuurivalem
Aldehüüdide üldine struktuurivalem
Näiteks saate sarnase protsessi käigus teada saada, kas lahus sisaldab glükoosi või fruktoosi. Glükoos annab positiivse tulemuse - saate "hõbepeegli", kuid fruktoos sisaldab ketoonirühma ja hõbeda sademe saamine on võimatu. Analüüsi läbiviimiseks on vaja formaldehüüdilahuse asemel lisada 10% glükoosilahust. Vaatame, miks ja kuidas lahustunud hõbe tahkeks sademeks muutub:
2OH + 3H2O + C6H12O6 (glükoos) = 2Ag↓+ 4NH3∙H2O + C6H12O7 (tekib glükoonhape).
Alustame sellest, et igal orgaaniliste ainete klassil on teatud reaktsioon, mille abil saab selle esindajaid teistest ainetest eristada. Kooli keemiakursus hõlmab kõigi orgaaniliste ainete põhiklasside kvaliteetsete reaktiivide uurimist.
Aldehüüdid: struktuursed omadused
Selle klassi esindajad on küllastunud süsivesinike derivaadid, milles radikaal on seotud aldehüüdrühmaga. Ketoonid on aldehüüdide isomeerid. Nende sarnasus seisneb nende kuulumises karbonüülühendite klassi. Kui sooritate ülesande, mis hõlmab aldehüüdi eraldamist segust, on vaja "hõbepeegli" reaktsiooni. Analüüsime selle keemilise muundamise omadusi ja selle rakendamise tingimusi. Hõbepeegli reaktsioon on hõbeda metalli redutseerimine hõbediamiini (1) hüdroksiidist. Lihtsustatud kujul on võimalik see keeruline ühend kirjutada hõbeoksiidi lihtsustatud kujul (1).
Karbonüülühendite eraldamine
Keerulise ühendi moodustamiseks lahustatakse hõbeoksiid ammoniaagis. Arvestades, et protsess on pöörduv reaktsioon, viiakse hõbepeegli reaktsioon läbi värskelt valmistatud hõbeoksiidi ammoniaagilahusega (1). Kui argentumi kompleksühend segatakse aldehüüdiga, toimub redoksreaktsioon. Protsessi lõppemisest annab märku metallilise hõbeda sadestumine. Kui etanaali ja hõbeoksiidi ammoniaagilahuse koostoime on õigesti läbi viidud, täheldatakse katseklaasi seintel hõbedase katte moodustumist. See oli visuaalne efekt, mis andis sellele interaktsioonile nime "hõbedane peegel".

Süsivesikute määramine
Hõbepeegli reaktsioon on kvalitatiivne aldehüüdrühmale, mistõttu orgaanilise keemia kursustel mainitakse seda ka süsivesikute nagu glükoosi äratundmise viisina. Arvestades selle aine spetsiifilist struktuuri, millel on aldehüüd-alkoholi omadused, on tänu “hõbepeegli” reaktsioonile võimalik eristada glükoosi fruktoosist, seega pole tegemist mitte ainult kvalitatiivse reaktsiooniga aldehüüdidele, vaid ka viis ära tunda paljusid teisi orgaaniliste ainete klasse.

"Hõbedase peegli" praktiline rakendamine
Näib, millised raskused võivad tekkida aldehüüdide ja hõbeoksiidi ammoniaagilahuse koosmõjul? Peate lihtsalt ostma hõbeoksiidi, varuma ammoniaaki ja valima aldehüüdi - ja võite katset ohutult alustada. Kuid selline primitiivne lähenemine ei vii teadlast soovitud tulemuseni. Katseklaasi seintel loodetud peegelpinna asemel näete (parimal juhul) tumepruuni hõbedast suspensiooni.

Interaktsiooni olemus
Kvaliteetne reaktsioon hõbedale eeldab teatud tegevusalgoritmi järgimist. Sageli isegi siis, kui ilmuvad peegelkihi märgid, jätab selle kvaliteet selgelt soovida. Mis on sellise ebaõnnestumise põhjused? Kas neid on võimalik vältida? Paljude probleemide hulgas, mis võivad põhjustada soovimatuid tulemusi, on kaks peamist:
- keemilise koostoime tingimuste rikkumine;
- halb pinna ettevalmistus hõbetamiseks.
Lahuses olevate lähteainete interaktsiooni käigus moodustuvad hõbekatioonid, mis ühinevad aldehüüdrühmaga, moodustades lõpuks kolloidsed väikesed hõbedaosakesed. Need terad on võimelised kleepuma klaasi külge, kuid neid saab lahuses säilitada hõbeda suspensioonina. Et tekiks osakeste adhesioon väärismetall klaasiga moodustub ühtlane ja vastupidav kiht, oluline on klaasi eelnev rasvatustamine. Ainult siis, kui katseklaasil on täiesti puhas algpind, võib loota ühtlase hõbedakihi moodustumisele.
Võimalikud probleemid
Suure saasteainena klaasnõud Tekib rasvane kate, millest tuleb lahti saada. Leeliselahus, aga ka kuum kroomisegu aitavad probleemi lahendada. Järgmisena pestakse katseklaasi destilleeritud veega. Kui leelist pole, võite kasutada sünteetiline aine nõude pesemiseks. Pärast rasvaärastuse lõpetamist pestakse klaasi tinakloriidi lahusega ja loputatakse veega. Lahuste valmistamiseks kasutatakse destilleeritud vett. Kui see pole saadaval, võite kasutada vihmavett. Redutseerivate ainetena kasutatakse glükoosi ja formaldehüüdi, mis võimaldavad lahusest puhta aine sadestumist. Aldehüüdiga on raske loota kvaliteetse hõbedase katte saamisele, kuid monosahhariid (glükoos) annab peegli pinnale ühtlase ja vastupidava hõbedakihi.

Järeldus
Hõbeklaasi jaoks on soovitatav kasutada hõbenitraati. Selle soola lahusele lisatakse leelist ja ammoniaagilahust. Hõbeda täieliku reaktsiooni ja klaasile ladestumise tingimus on leeliselise keskkonna loomine. Aga kui seda reaktiivi on liiga palju, kõrvalmõjud. Sõltuvalt valitud katsetehnikast saadakse kuumutamisel kvaliteetne reaktsioon. Lahuse värvimine sisse Pruun värv näitab hõbeda pisikeste kolloidosakeste moodustumist. Järgmisena ilmub klaasi pinnale peegelkate. Kui protsess õnnestub, on metallikiht sile ja vastupidav.
Enne keemilise eksperimendi alustamist tuleb välja selgitada, mis on aldehüüd, mille olemasolu tahetakse kindlaks teha. Aldehüüdid on rühm orgaanilisi ühendeid, milles süsinikuaatomil on kaksikside hapnikuaatomiga. Iga selline ühend sisaldab >C=O rühma. Reaktsiooni olemus seisneb selles, et selle tulemusena moodustub metalliline hõbe, mis ladestub pinnale. Reaktsioon viiakse läbi ainetega, mis sisaldavad kuumutamisel vesilahuses aldehüüdrühma ammoniaagi juuresolekul. Kõige sagedamini kasutatakse reaktsioonis suhkrut ja aldehüüdina tavalist suhkrut. Tavaliselt kasutatakse ammoniaaki sisaldavat ainet.Hõbedasooladega töötades peate olema ettevaatlik, kuna need jätavad mustad jäljed. Tehke katse kinnastega.
Kuidas reaktsioon tekib?
?Katse jaoks vajalikke reaktiive võib leida igast apteegist. Hõbenitraat on lapise pliiats. Sealt saab osta ka formaldehüüdi ja ammoniaaki. Muuhulgas vajate keemilisi klaasnõusid. Ained, millega peate tegelema, ei ole agressiivsed, kuid kõik keemilised katsed on kõige parem läbi viia keemilisest klaasist valmistatud katseklaasides ja -kolbides. Loomulikult tuleb nõud põhjalikult pesta. Valmistage hõbenitraadi AgNO3 vesilahus. Lisage sellele ammoniaak, see tähendab ammooniumhüdroksiid NH4OH. Te moodustate hõbeoksiidi Ag2O, mis sadestub pruuni sadena. Seejärel muutub lahus selgeks ja moodustub OH kompleks. Just tema mõjutab redoksreaktsiooni käigus aldehüüdi, mille tulemusena moodustub ammooniumsool. Selle reaktsiooni valem näeb välja selline: R-CH=O + 2OH --> RCOONH4 + 2Ag +3NH3 + H2O. Kui jätate reaktsiooni ajaks purki klaaspulga või -taldriku, kattub see umbes päeva pärast läikiva kihiga. Sama kiht moodustub anuma seintele.
Reaktsiooni saab kirjutada lihtsustatult: R-CH=O + Ag2O --> R-COOH + 2Ag.
Kuidas peeglid tehti
Enne pihustusmeetodi tulekut oli hõbepeegli reaktsioon ainus viis peeglite saamine klaasile ja portselanile. Praegu kasutatakse seda meetodit juhtiva kihi saamiseks klaasile, keraamikale ja muudele dielektrikutele. Seda tehnoloogiat kasutatakse kaetud optika loomiseks fotoobjektiividele, teleskoopidele jne.Laboritöö nr 5
Omadusedsüsivesikuid
Katse 1. Hõbedase peegli reaktsioon on taastumisreaktsioon hõbedane ammoniaagi lahusest hõbeoksiid (Tollensi reaktiiv).
Vesilahuses ammoniaak hõbeoksiid lahustub, moodustades kompleksühendi - diamiinhõbe(I)hüdroksiidi OH
kui millele lisada aldehüüd toimub redoksreaktsioon, mille käigus moodustub metallist hõbe:
Kui reaktsioon viiakse läbi puhaste ja siledate seintega anumas, sadestub hõbe õhukese kile kujul, moodustades peegelpinna.
Väikseima saastumise korral eraldub hõbe halli lahtise sette kujul.
"Hõbepeegli" reaktsiooni saab kasutada aldehüüdide kvalitatiivse reaktsioonina. Seega saab "hõbepeegli" reaktsiooni kasutada eristavaks reaktsiooniks glükoos Ja fruktoos. Glükoos on aldoos (sisaldab avatud kujul aldehüüdrühma) ja fruktoos on ketoos (sisaldab ketorühma avatud kujul). Seetõttu annab glükoos “hõbepeegli” reaktsiooni, kuid fruktoos mitte. Aga kui lahuses on leeliseline keskkond, siis ketoosid isomeriseeruvad aldoosideks ja annavad positiivseid reaktsioone ka ammoniaagilahusega. hõbeoksiid (Tollensi reaktiiv).
Glükoosi kvalitatiivne reaktsioon hõbeoksiidi ammoniaagilahusega. Aldehüüdrühma olemasolu glükoosis saab tõestada hõbeoksiidi ammoniaagilahusega. Hõbeoksiidi ammoniaagilahusele lisage glükoosilahus ja kuumutage segu veevannis. Varsti hakkab kolvi seintele ladestuma metallist hõbedat. Seda reaktsiooni nimetatakse hõbepeegli reaktsiooniks. Seda kasutatakse kvaliteetse ühendina aldehüüdide avastamiseks. Glükoosi aldehüüdrühm oksüdeeritakse karboksüülrühmaks. Glükoos muudetakse glükoonhappeks.
CH 2 TEMA – (SNON) 4 – SLEEP +Ag 2 O= CH 2 TEMA – (SNON) 4 – COOH + 2Ag↓

Töö järjekord.
2 ml valatakse kahte katseklaasi. hõbeoksiidi ammoniaagilahus. Lisage ühele neist 2 ml. 1% glükoosilahus, teine - fruktoos. Mõlemad katseklaasid keevad.
Hõbeoksiidhüdraadi ammoniaagilahus saadakse hõbenitraadi reageerimisel naatriumhüdroksiidi ja ammooniumhüdroksiidiga:
AgNO3+ NaOH → AgOH↓+ NaNO3,
AgOH + 2 NH4 OH → [ Ag(NH3)2] OH + H2O,
ammoniaagi lahus
OH + 3 H2 → Ag2O + 4 NH4 OH.
Meetodi põhimõte. Katseklaasi seintele tekib metallilise hõbeda eraldumise tulemusena glükoosiga peegel.
Töö kujundus: Kirjutage vihikusse järeldus, reaktsiooni käik ja võrrandid.
Katse 3. Kvalitatiivne reaktsioon fruktoosile
Meetodi põhimõte. Fruktoosi sisaldava proovi kuumutamisel juuresolekul resortsinool Ja vesinikkloriidhappest kuni 80 o C ilmub mõne aja pärast fruktoosiga katseklaasi erkpunane värvus.
Fruktoosi sisaldava proovi kuumutamisel juuresolekul resortsinool Ja vesinikkloriidhappest ilmub kirsipunane värv. Proov on kasutatav ka muu tuvastamiseks ketoos. Aldose samadel tingimustel suhtlevad nad aeglasemalt ja annavad kahvaturoosa värvi või ei suhtle üldse. Avatud F. F. Selivanov aastal 1887. Kasutatakse uriini analüüsiks. Test on positiivne metaboolse või transpordiga seotud fruktosuuria suhtes. Puuviljade ja mee toidukoormuse korral on test positiivne 13% juhtudest. Chem. valem fruktoos – C6H12O6
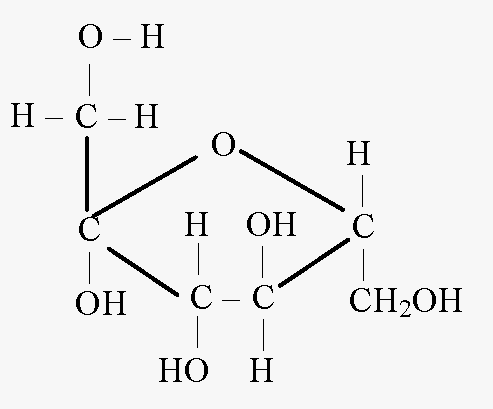
Fruktoosi tsükliline valem
Atsükliline vorm 
fruktoos
Värvitud ühendus
R- jäägid
hüdroksümetüülfurfuraal
Töö järjekord.
2 ml valatakse kahte katseklaasi: ühte - 1% glükoosilahus, teise - 1% fruktoosilahus. Mõlemasse katseklaasi lisatakse 2 ml Selivanovi reaktiivi: 0,05 g resortsinooli lahustatakse 100 ml 20% vesinikkloriidhappes. Mõlemad katseklaasid kuumutatakse ettevaatlikult 80 o C-ni (enne keetmist). Ilmub punane värv.

Järeldused: katse tulemused ja reaktsioonivõrrand kirjutatakse vihikusse.
Jätkame keemiakatsetuste teemat, sest loodame, et need meeldivad teile kindlasti. Seekord toome teie tähelepanu alla veel ühe põneva kogemuse, mille käigus saame hõbedase peegli.
Alustame video vaatamisega
Meil on vaja:
- mahutavus;
- hõbenitraat;
- kuum vesi;
- ammoniaagilahus 10%;
- glükoos;
- alkoholipõleti

Alustame hõbenitraadiga. Võtke seda umbes gramm ja lahjendage väikeses koguses kuum vesi.

Seejärel lisage saadud lahusele naatriumhüdroksiid. Selle reaktsiooni käigus moodustub hõbeoksiid, mis sadestub.

Järgmisena lisage hõbeoksiidi sademele 10-protsendiline ammoniaagilahus. Ammoniaagilahust tuleb lisada, kuni sade lahustub.

Selle reaktsiooni käigus moodustub hõbedane ammoniaak. Lisage saadud lahusele 5 grammi glükoosi.

Nüüd peate saadud segu kuumutama. Selleks süüdake alkoholipõleti ja asetage sellele klaas, nii et segu järk-järgult soojeneb. Selle reaktsiooni käigus vabaneb väga palju suur hulk ammoniaak, seega tuleb see reaktsioon läbi viia kas kapoti all või väljas. Reaktsiooni käigus võib tekkida ka hõbenitrit, mis on väga ohtlik aine, nii et nõud tuleb pärast reaktsiooni põhjalikult pesta.


Mõne aja pärast hakkab klaasi seintele tasapisi ladestuma õhuke hõbedakiht. Reaktsioon lõppes ligikaudu 15 minutit pärast kuumutamise algust.


Ühtlasema hõbedakihi saamiseks tuleb panna klaas seguga suurde anumasse, valada anumasse kuum vesi ja asetada see piiritusepõletile. Nii jaotub temperatuur ühtlaselt ja tulemus on tõhusam.