Каква е реакцията на сребърното огледало? Химичен експеримент: получаване на сребърно огледало. Условия за реакция на сребърно огледало
Експериментът с красивия ефект от образуването на огледално покритие върху стъкло е много визуален. Тази реакция изисква опит и търпение. В тази статия ще научите за необходимата и специфична подготовка на оборудването, както и ще видите какви уравнения на реакцията протича този процес.
Същността на реакцията на сребърното огледало е образуването на метално сребро в резултат на редокс реакция по време на взаимодействието на амонячен разтвор на сребърен оксид в присъствието на алдехиди.
"Сребърно огледало" (епруветка отляво)За да създадете издръжлив сребърен слой, ще ви трябва:
- стъклена колба с вместимост до 100 ml;
- разтвор на амоняк (2,5-4%);
- сребърен нитрат (2%);
- воден разтвор на формалдехид (40%).
Вместо и можете да вземете готовия реактив на Толенс - разтвор на амоняксребърен оксид. За да го създадете, трябва да добавите 1 грам сребърен нитрат към 10 капки вода (ако течността ще се съхранява дълго време, трябва да я поставите на тъмно място или в стъклен съд с тъмни стени). Непосредствено преди експеримента разтворът (около 3 ml) трябва да се смеси в съотношение 1:1 с 10% воден разтвор на натриев хидроксид. Среброто може да се утаи, така че се разрежда чрез бавно добавяне на амонячен разтвор. Препоръчваме да проведете още един грандиозен експеримент с разтвор на амоняк и да отпечатате „химическа снимка“.
Реакцията се провежда при стайна температура. Задължително условиеуспешен финал е идеално чисти и гладки стени на стъкления съд. Ако по стените има и най-малките частици замърсители, утайката, получена в резултат на експеримента, ще се превърне в рохкав слой от черен или тъмносив цвят.
За да почистите колбата, която трябва да използвате различни видовеалкални разтвори , Така че за обработка можете да вземете разтвор, който след почистване трябва да се измие с дестилирана вода. Необходимо е многократно да се изплаква колбата от почистващия препарат.
Защо чистотата на съдовете е толкова важна?
Факт е, че колоидните сребърни частици, образувани в края на експеримента, трябва да се придържат здраво към повърхността на стъклото. По повърхността му не трябва да има мазнини или механични частици. водата не съдържа соли и е идеална за окончателно почистване на колбата. Може да се приготви у дома, но е по-лесно да се купи готова течност.
Уравнение на реакцията на сребърно огледало:
Ag₂O + 4 NH3·Н2О ⇄ 2ОН + 3Н₂О,
където OH е диамин сребърен хидроксид, получен чрез разтваряне на металния оксид във воден разтвор на амоняк.
 Диаминна сребърна комплексна молекула
Диаминна сребърна комплексна молекула
важно!Реакцията работи при ниски концентрации на амоняк - внимателно спазвайте пропорциите!
Ето как протича последният етап на реакцията:
R (всеки алдехид)-CH=O + 2OH → 2Ag (утаен сребърен колоид) ↓ + R-COONH₄ + 3NH3 + H₂O
По-добре е вторият етап от реакцията да се извърши чрез внимателно нагряване на колбата над пламъка на горелката - това ще увеличи шансовете експериментът да бъде успешен.
Какво може да покаже реакцията на сребърно огледало?
Тази интересна химическа реакция не само демонстрира определени състояния на дадено вещество - тя може да се използва за извършване на качествено определяне на алдехиди. Тоест, такава реакция ще реши въпроса: дали има алдехидна група в разтвора или не.
 Обща структурна формула на алдехиди
Обща структурна формула на алдехиди
Например, в подобен процес можете да разберете дали даден разтвор съдържа глюкоза или фруктоза. Глюкозата ще даде положителен резултат - ще получите "сребърно огледало", но фруктозата съдържа кетонна група и е невъзможно да се получи сребърна утайка. За да се извърши анализът, вместо разтвор на формалдехид е необходимо да се добави 10% разтвор на глюкоза. Нека да разгледаме защо и как разтвореното сребро се превръща в твърда утайка:
2OH + 3H₂O + C₆H₁₂O₆ (глюкоза) = 2Ag↓+ 4NH3₃∙H₂O + C₆H₁₂O₇ (образува се глюконова киселина).
Да започнем с факта, че всеки клас органични вещества има определена реакция, с помощта на която неговите представители могат да бъдат разграничени от другите вещества. Училищният курс по химия включва изучаване на всички висококачествени реактиви за основните класове органични вещества.
Алдехиди: структурни характеристики
Представители на този клас са производни на наситени въглеводороди, в които радикалът е свързан с алдехидна група. Кетоните са изомери на алдехиди. Тяхното сходство се състои в принадлежността им към класа на карбонилните съединения. Когато изпълнявате задача, която включва изолиране на алдехид в смес, ще е необходима реакция на "сребърно огледало". Нека анализираме характеристиките на тази химична трансформация, както и условията за нейното осъществяване. Реакцията със сребърно огледало е процесът на редукция на метал сребро от сребърен диамин(1) хидроксид. В опростена форма е възможно това комплексно съединение да се напише в опростената форма на сребърен оксид (1).
Разделяне на карбонилни съединения
За да се образува комплексно съединение, сребърният оксид се разтваря в амоняк. Като се има предвид, че процесът е обратима реакция, реакцията със сребърно огледало се извършва с прясно приготвен амонячен разтвор на сребърен оксид (1). Когато сложно съединение на аргентум се смеси с алдехид, възниква окислително-редукционна реакция. Завършването на процеса се показва от утаяването на метално сребро. При правилно взаимодействие на етанал и амонячен разтвор на сребърен оксид се наблюдава образуване на сребърно покритие по стените на епруветката. Именно визуалният ефект даде на това взаимодействие името „сребърно огледало“.

Определяне на въглехидрати
Реакцията на сребърно огледало е качествена към алдехидна група, така че в курсовете по органична химия се споменава и като начин за разпознаване на въглехидрати като глюкоза. Като се има предвид специфичната структура на това вещество, което проявява свойствата на алдехид-алкохол, благодарение на реакцията на „сребърно огледало" е възможно да се разграничи глюкозата от фруктозата. По този начин това е не само качествена реакция към алдехиди, но и начин за разпознаване на много други класове органични вещества.

Практическо приложение на „сребърното огледало“
Изглежда, какви трудности могат да възникнат при взаимодействието на алдехиди и амонячен разтвор на сребърен оксид? Просто трябва да закупите сребърен оксид, да се запасите с амоняк и да изберете алдехид - и можете спокойно да започнете експеримента. Но такъв примитивен подход няма да доведе изследователя до желания резултат. Вместо очакваната огледална повърхност по стените на епруветката ще видите (в най-добрия случай) тъмнокафява сребриста суспензия.

Същността на взаимодействието
Висококачествената реакция към среброто предполага спазване на определен алгоритъм на действия. Често, дори когато се появят признаци на огледален слой, качеството му очевидно оставя много да се желае. Какви са причините за такъв провал? Възможно ли е да ги избегнем? Сред многото проблеми, които могат да доведат до нежелани резултати, има два основни:
- нарушаване на условията за химично взаимодействие;
- лоша подготовка на повърхността за посребряване.
По време на взаимодействието на изходните вещества в разтвора се образуват сребърни катиони, които се свързват с алдехидната група, като в крайна сметка образуват колоидни малки частици сребро. Тези зърна могат да се придържат към стъкло, но могат да бъдат запазени в разтвор като сребърна суспензия. За да се получи адхезия на частиците благороден металсъс стъкло се образува равномерен и издръжлив слой, важно е стъклото да се обезмасли предварително. Само при идеално чиста начална повърхност на епруветката може да се разчита на образуването на равномерен сребърен слой.
Възможни проблеми
Като основен замърсител стъклени изделияИма мазно покритие, от което трябва да се отървете. Алкален разтвор, както и гореща хромова смес ще помогнат за решаването на проблема. След това епруветката се измива с дестилирана вода. Ако няма алкали, можете да използвате синтетичен агентза миене на съдове. След приключване на обезмасляването стъклото се измива с разтвор на калаен хлорид и се изплаква с вода. За приготвяне на разтвори се използва дестилирана вода. Ако не е налице, можете да използвате дъждовна вода. Глюкозата и формалдехидът се използват като редуциращи агенти, които позволяват утаяването на чисто вещество от разтвор. С алдехид е трудно да се разчита на получаване на висококачествено сребърно покритие, но монозахаридът (глюкоза) дава равномерен и издръжлив сребърен слой върху повърхността на огледалото.

Заключение
За сребърно стъкло е препоръчително да използвате сребърен нитрат. Към разтвора на тази сол се добавят алкален и амонячен разтвор. Условието за пълна реакция и отлагане на сребро върху стъкло е създаването на алкална среда. Но ако има излишък от този реагент, странични ефекти. В зависимост от избраната експериментална техника чрез нагряване се получава висококачествена реакция. Оцветяване на разтвора в кафяв цвятпоказва образуването на малки колоидни частици сребро. След това върху повърхността на стъклото се появява огледално покритие. Ако процесът е успешен, металният слой ще бъде гладък и издръжлив.
Преди да започнете химичен експеримент, е необходимо да разберете какъв е алдехидът, чието присъствие трябва да се определи. Алдехидите са група органични съединения, в които въглеродният атом има двойна връзка с кислороден атом. Всяко такова съединение съдържа >C=O група. Същността на реакцията е, че в резултат на това се образува метално сребро, което се отлага на повърхността. Реакцията се провежда с вещества, съдържащи алдехидна група във воден разтвор при нагряване, в присъствието на амоняк. Най-често в реакцията се използва захар, а като алдехид се използва обикновена захар. Обикновено се използва веществото, съдържащо амоняк.Трябва да внимавате, когато работите със сребърни соли, тъй като те оставят черни следи. Извършете експеримента с ръкавици.
Как протича реакцията?
?Реактивите за експеримента могат да бъдат намерени във всяка аптека. Сребърният нитрат е лапис молив. Там също можете да закупите формалдехид и амоняк. Освен всичко друго, имате нужда от химически стъклени съдове. Веществата, с които ще трябва да се справите, са неагресивни, но всякакви химични експерименти е най-добре да се провеждат в епруветки и колби, направени от химическо стъкло. Разбира се, съдовете трябва да се измият старателно. Направете воден разтвор на сребърен нитрат AgNO3. Добавете към него амоняк, тоест амониев хидроксид NH4OH. Образувате сребърен оксид Ag2O, който се утаява като кафява утайка. След това разтворът става бистър и се образува ОН комплекс. Той е този, който действа върху алдехида по време на редокс реакцията, което води до образуването на амониева сол. Формулата за тази реакция изглежда така: R-CH=O + 2OH --> RCOONH4 + 2Ag +3NH3 + H2O. Ако оставите стъклена пръчка или чиния в буркана по време на реакцията, след около ден тя ще се покрие с лъскав слой. Същият слой се образува и по стените на съда.
Реакцията може да бъде написана по опростен начин: R-CH=O + Ag2O --> R-COOH + 2Ag.
Как са направени огледалата
Преди появата на метода на разпръскване, реакцията на сребърно огледало беше единствения начинполучаване на огледала върху стъкло и порцелан. В момента този метод се използва за получаване на проводящ слой върху стъкло, керамика и други диелектрици. Тази технология се използва за създаване на оптика с покритие за фотографски лещи, телескопи и др.Лабораторна работа № 5
Имотивъглехидрати
Опит 1. Реакция на сребърно огледалое реакция на възстановяване среброот амонячен разтвор сребърен оксид (реактив на Толенс).
Във воден разтвор амоняксребърен оксид се разтваря и образува комплексно съединение - диамин сребърен(I) хидроксид ОН
когато се добави към който алдехидвъзниква окислително-редукционна реакция за образуване на метално сребро:
Ако реакцията се проведе в съд с чисти и гладки стени, тогава среброто се утаява под формата на тънък филм, образувайки огледална повърхност.
При най-малкото замърсяване среброто се отделя под формата на сива рохкава утайка.
Реакцията на "сребърно огледало" може да се използва като качествена реакция за алдехиди. По този начин реакцията на „сребърно огледало“ може да се използва като отличителна между тях глюкозаИ фруктоза. Глюкозата е алдоза (съдържа алдехидна група в отворена форма), а фруктозата е кетоза (съдържа кето група в отворена форма). Следователно глюкозата дава реакция на „сребърно огледало“, но фруктозата не. Но ако в разтвора присъства алкална среда, тогава кетозите се изомеризират в алдози и също дават положителни реакции с разтвор на амоняк сребърен оксид (реактив на Толенс).
Качествена реакция на глюкоза с амонячен разтвор на сребърен оксид.Наличието на алдехидна група в глюкозата може да се докаже с помощта на амонячен разтвор на сребърен оксид. Добавете разтвор на глюкоза към амонячен разтвор на сребърен оксид и загрейте сместа на водна баня. Скоро металното сребро започва да се отлага по стените на колбата. Тази реакция се нарича реакция на сребърно огледало. Използва се като качествено съединение за откриване на алдехиди. Алдехидната група на глюкозата се окислява до карбоксилна група. Глюкозата се превръща в глюконова киселина.
CH 2 ТОЙ – (SNON) 4 – СЪН +Ag 2 О= СН 2 ТОЙ – (SNON) 4 – COOH + 2Ag↓

Редът на работа.
В две епруветки се наливат по 2 ml. амонячен разтвор на сребърен оксид. Към един от тях добавете 2 мл. 1% разтвор на глюкоза, другият - фруктоза. И двете епруветки кипят.
Амонячен разтвор на сребърен оксид хидрат се получава чрез взаимодействие на сребърен нитрат с натриев хидроксид и амониев хидроксид:
AgNO3+ NaOH → AgOH↓+ NaNO3,
AgOH + 2 NH4 OH→[ Ag(NH3)2] OH + H2O,
разтвор на амоняк
OH + 3 H2→ Ag2O + 4 NH4 OH.
Принцип на метода. По стените на епруветката с глюкоза се образува огледало в резултат на отделянето на метално сребро.
Оформяне на работата: Напишете извода, както и протичането и уравненията на реакцията в тетрадка.
Опит 3. Качествена реакция на фруктоза
Принцип на метода. При нагряване на проба, съдържаща фруктоза в присъствието резорцинолИ на солна киселинадо 80 o C след известно време в епруветката с фруктоза се появява яркочервен цвят.
При нагряване на проба, съдържаща фруктоза в присъствието резорцинолИ на солна киселинапоявява се вишневочервен цвят. Пробата е приложима и за откриване на други кетоза. Алдозапри същите условия те взаимодействат по-бавно и дават бледорозов цвят или изобщо не си взаимодействат. Отворете Ф. Ф. Селивановпрез 1887 г. Използва се за анализ на урината. Тестът е положителен за фруктозурия от метаболитен или транспортен произход. В 13% от случаите тестът е положителен при хранително натоварване с плодове и мед. Chem. формулафруктоза – C 6 H 12 O 6
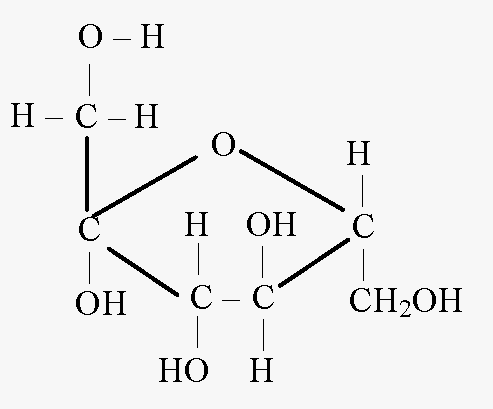
Циклична формула на фруктоза
Ациклична форма 
фруктоза
Боядисана връзка
R- остатъци
хидроксиметилфурфурол
Редът на работа.
2 ml се наливат в две епруветки: в едната - 1% разтвор на глюкоза, в другата - 1% разтвор на фруктоза. Към двете епруветки се добавят 2 ml реактив на Селиванов: 0,05 g резорцинол се разтварят в 100 ml 20% солна киселина. И двете епруветки се загряват внимателно до 80 o C (преди кипене). Появява се червен цвят.

Изводи: резултатите от опита и уравнението на реакцията се записват в тетрадка.
Нека продължим темата за химичните експерименти, защото се надяваме, че определено ще ви харесат. Този път представяме на вашето внимание още едно завладяващо преживяване, по време на което ще получим сребърно огледало.
Нека започнем с гледане на видеото
Ще ни трябва:
- капацитет;
- сребърен нитрат;
- топла вода;
- разтвор на амоняк 10%;
- глюкоза;
- спиртна горелка

Да започнем със сребърен нитрат. Вземете около грам от него и го разредете в малко количество топла вода.

След това добавете натриев хидроксид към получения разтвор. По време на тази реакция се образува сребърен оксид, който се утаява.

След това добавете 10 процента разтвор на амоняк към утайката от сребърен оксид. Разтворът на амоняк трябва да се добави, докато утайката се разтвори.

По време на тази реакция се образува сребърен амоняк. Добавете 5 грама глюкоза към получения разтвор.

Сега трябва да загреете получената смес. За да направите това, запалете спиртната горелка и поставете чашата върху нея, така че сместа постепенно да се нагрява. По време на тази реакция се освобождава много голям бройамоняк, така че тази реакция трябва да се проведе или под капак, или навън. Реакцията може също да произведе сребърен нитрит, който е много опасно вещество, така че съдовете трябва да се измият добре след реакцията.


След известно време тънък слой сребро постепенно започва да се утаява по стените на чашата. Реакцията завършва приблизително 15 минути след началото на нагряването.


За да получите по-равномерен слой сребро, трябва да поставите чаша със сместа в голям съд, да налеете гореща вода в съда и да го поставите върху спиртна горелка. Така температурата ще се разпредели равномерно и резултатът ще бъде по-ефективен.